Ya que está llegando el día de la madre hoy os quiero hablar sobre las mitocondrias y su ADN, ya que este se hereda solo por vía materna.
Empecemos por definir que son las mitocondrias.
Son pequeños orgánulos que se encuentran en el interior de las células y cuya función principal es la de producir energía en forma de ATP a partir de la oxidación de nutrientes que se encuentran en los alimentos.
Una de las peculiaridades de las mitocondrias es que tienen un origen endosimbionte.
En algún momento de la evolución una bacteria de vida libre (de la familia de las alfaprotrobacterias) fue absorbida por una célula, estableciéndose una relación de simbiosis entre ambas.
Esta célula primitiva, ancestro de los eucariotas (plantas, animales y nosotros mismos) se cree que pertenecía al grupo de las arqueas (existen tres dominios a nivel taxonómico: los eucariotas, las bacterias y las arqueas).
Todas los organismos eucariotas tienen mitocondrias en su interior, lo que demuestra la importancia que tuvo este proceso de endosimbiosis en la evolución.
Presentan dos membranas, una externa y otra interna con múltiples crestas (para aumentar su superficie). En la matriz se produce el Ciclo de Krebs y la oxidación de los ácidos grasos, mientras que en la membrana interna se produce la fosforilación oxidativa (son tres procesos claves en la obtención de energía).
En la matriz también se encuentra el ADN mitocondrial (uno de los hechos que demuestra que las mitocondrias tienen un origen bacteriano, al igual que la existencia de dos membranas y el tipo de ribosomas que se encuentras en ellas).
Este ADN es circular, al menos en vertebrados, (el ADN del núcleo de las células es lineal), de pequeño tamaño y hay varias copias en cada mitocondria.
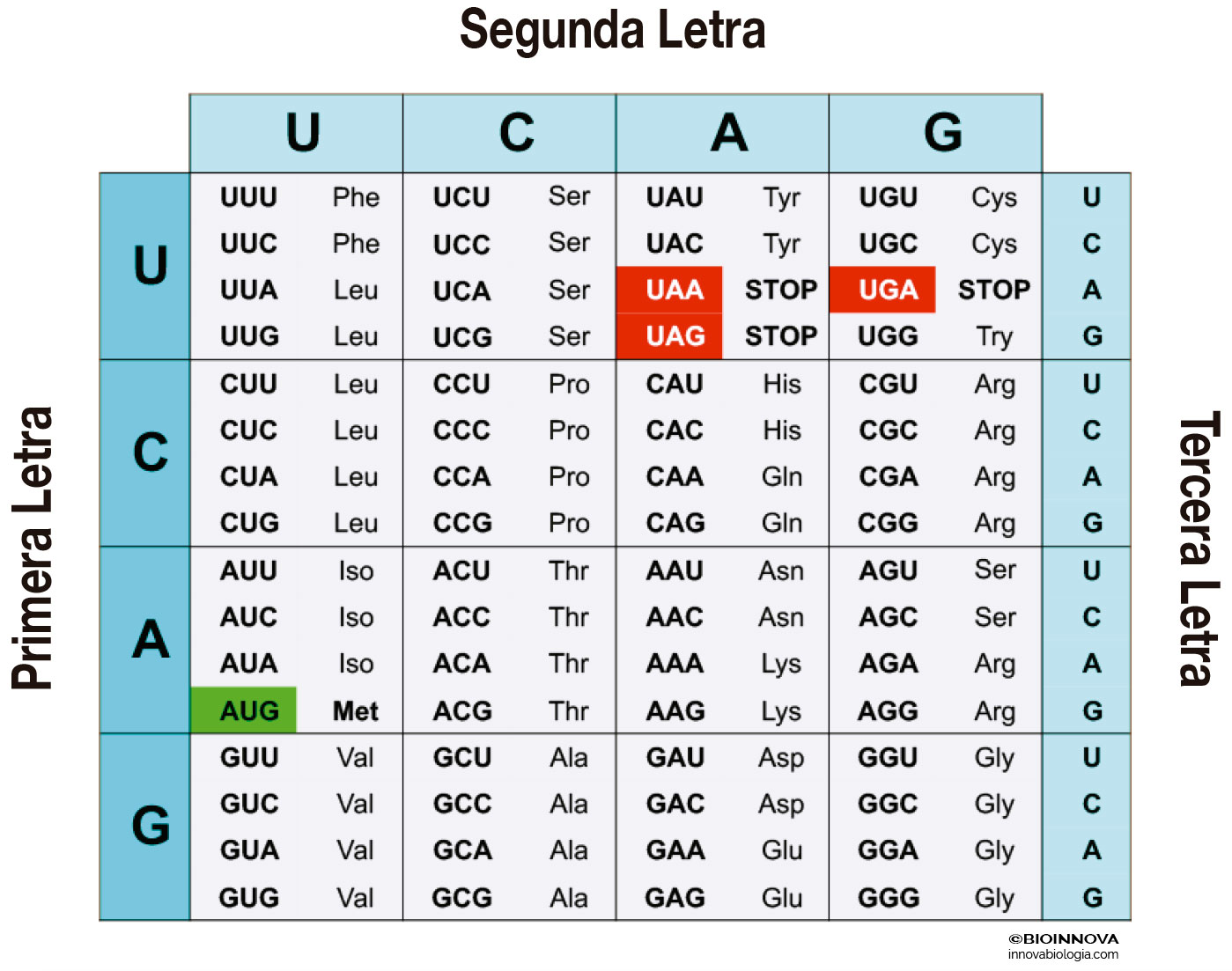
Se han descrito 37 genes, que codifican varias proteínas necesarias para la función de las mitocondrias, como algunos enzimas que participan en la respiración y la maquinaria necesaria para que se produzca la traducción del ADN a proteínas.
Y debido a que solo se heredan por vía materna, ya que es el óvulo el que aporta las mitocondrias al cigoto tras la fecundación. Esto implica que el ADN de nuestras mitocondrias es como el ADN de las mitocondrias de nuestras madres. Por ello se utiliza en el estudio de parentescos y en genética evolutiva.
De estos estudios surge lo que se conoce como “Eva mitocondrial”, la que sería la última antecesora común del ser humano moderno . Se estima que esta Eva vivió en el sur de África hace unos 200.000 años, en la región al sur del río Zambeze (Zambia, Angola, Namibia, Botsuana, …).
Es un concepto que se refiere a un linaje, no hay que entenderla como a la Eva del cristianismo.
Esas primeras poblaciones humanas se mantuvieron estables unos 70.000 años, momento en el cual aparecen nuevos linajes (hace 130.000 – 110.000 años).
En ese momento debido a un cambio en el clima se cree que se abrieron corredores verdes que posibilitaron las migraciones de diferentes grupos hacia Asia y Europa.
También se habló hace unos años las siete Evas de Europa, que serían los linajes que han dado lugar a todo los europeos actuales, con una antigüedad que va desde los 45.000 años a los 10.000 años. Una de estas Evas tendría su origen en España.
Estos estudios generan mucha controversia ya que solo se mira una pequeña parte del genoma y quizás este ADN mitocondrial solo nos esté dando una información incompleta.
Pero analizar el ADN nuclear para este tipo de estudios aún resulta muy complejo, por su gran tamaño y porque también interviene el genoma paterno.
Así que el árbol genealógico del ser humano aún está muy lejos de estar claro (aunque nuestro origen africano es un hecho, por si algún lector tenía dudas al respecto).
El estudio de este ADN mitocondrial también es importante en medicina debido a que hay varias enfermedades causadas por mutaciones. También es muy importante el papel de las mitocondrias en el crecimiento de los tumores.
Fuentes:
- http://www3.uah.es/chemevol/index.php/2021/02/03/dna-mitocondrial-y-enfermedades-relacionadas-2/
- https://elpais.com/diario/2000/04/20/sociedad/956181604_850215.html
- https://www.nationalgeographic.es/ciencia/2019/10/polemico-estudio-senala-origen-humanidad-botsuana
- https://elpais.com/diario/2000/04/20/sociedad/956181604_850215.html
- https://www.bbc.com/mundo/noticias-50222475